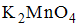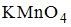Используя метод электронного баланса составьте уравнение реакции Соотнесите формулы окислителя восс...: ответ на тест 1161216 - Химия
Используя метод электронного баланса, составьте уравнение реакции 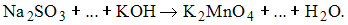
Соотнесите формулы окислителя, восстановителя и общую сумму коэффициентов в уравнении реакции.
1. Формула окислителя
2. Формула восстановителя
3. Общая сумма коэффициентов
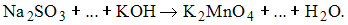
Соотнесите формулы окислителя, восстановителя и общую сумму коэффициентов в уравнении реакции.
1. Формула окислителя
2. Формула восстановителя
3. Общая сумма коэффициентов
Вопрос задал(а): Анонимный пользователь, 13 Ноябрь 2020 в 21:01
На вопрос ответил(а): Анастасия Степанова, 13 Ноябрь 2020 в 21:01
На вопрос ответил(а): Анастасия Степанова, 13 Ноябрь 2020 в 21:01