Промышленное получение некоторых простых веществ металлов водорода и др. основано на окислительно-во...: ответ на тест 1165041 - Химия
Промышленное получение некоторых простых веществ (металлов, водорода и др.) основано на окислительно-восстановительных реакциях их оксидов с углеродом, в которых углерод является и реагентом-восстановителем, и реагентом-источником тепловой энергии. Другие методы их получения и дальнейшее использование образующихся продуктов определяются их физическими, химическими свойствами и условиями проведения реакций.
В процессе получения олова в промышленности возможно использование реакции угля с оксидом олова (II)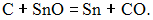 Теплота, необходимая для осуществления процесса, обеспечивается горением углерода. Если энтальпии образования оксида олова (II), угарного и углекислого газов равны: –286, –111 и –394 кДж/моль соответственно, то для получения 1785 кг олова потребуется ____ кг углерода.
Теплота, необходимая для осуществления процесса, обеспечивается горением углерода. Если энтальпии образования оксида олова (II), угарного и углекислого газов равны: –286, –111 и –394 кДж/моль соответственно, то для получения 1785 кг олова потребуется ____ кг углерода.
(Потерями углерода на побочные процессы пренебречь; ответ привести с точностью до целого значения; Ar(Sn) = 119.)
В процессе получения олова в промышленности возможно использование реакции угля с оксидом олова (II)
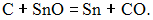 Теплота, необходимая для осуществления процесса, обеспечивается горением углерода. Если энтальпии образования оксида олова (II), угарного и углекислого газов равны: –286, –111 и –394 кДж/моль соответственно, то для получения 1785 кг олова потребуется ____ кг углерода.
Теплота, необходимая для осуществления процесса, обеспечивается горением углерода. Если энтальпии образования оксида олова (II), угарного и углекислого газов равны: –286, –111 и –394 кДж/моль соответственно, то для получения 1785 кг олова потребуется ____ кг углерода.(Потерями углерода на побочные процессы пренебречь; ответ привести с точностью до целого значения; Ar(Sn) = 119.)
Вопрос задал(а): Анонимный пользователь, 13 Ноябрь 2020 в 21:03
На вопрос ответил(а): Анастасия Степанова, 13 Ноябрь 2020 в 21:03
На вопрос ответил(а): Анастасия Степанова, 13 Ноябрь 2020 в 21:03
